巴氏吸管由醫用級聚乙烯(PE)制成,管體
2017年11月CRISPR/Cas亮點盤點
2017年11月30日//---基因組編輯技術CRISPR/Cas9被《科學》雜志列為2013年年度科技進展之一,受到人們的高度重視。CRISPR是規律間隔性成簇短回文重復序列的簡稱,Cas是CRISPR相關蛋白的簡稱。CRISPR/Caszui初是在細菌體內發現的,是細菌用來識別和摧毀抗噬菌體和其他病原體入侵的防御系統。
即將過去的11月份,有哪些重大的CRISPR/Cas研究或發現呢?小編梳理了一下這個月生物谷報道的CRISPR/Cas研究方面的新聞,供大家閱讀。
1.Nat Commun:新方法使得CRISPR基因編輯準確性高達98%
doi:10.1038/s41467-017-01875-9

如今,在一項新的研究中,美國威斯康星大學麥迪遜分校生物醫學工程教授Krishanu Saha領導的一個研究團隊開發出一種能夠讓這種修復不那么容易地出錯的新方法。相關研究結果于2017年11月23日在線發表在Nature Communications期刊上,論文標題為“Assembly of CRISPR ribonucleoproteins with biotinylated oligonucleotides via an RNA aptamer for precise gene editing”。
與標準的CRISPR技術相比,這種新方法將按照所希望的那樣地重寫DNA序列的概率提高了10倍。這些研究人員利用一種被稱作RNA適配子(RNA aptamer)的分子膠組裝一種完整的CRISPR修復工具包并將這種工具包運送DNA切割位點上,從而實現這種更高的修復度。
與現有技術相比,新方法還有其他的幾項優勢。首先,這種工具包僅含有非病毒試劑,這就簡化了生產過程,并降低了在未來開展遺傳手術臨床應用時存在的安全性問題。其次,將一種RNA適配子添加到這種工具包中要比修飾Cas9蛋白更加容易,而且提供更大的靈活性。通過添加熒光標記,這允許研究人員很容易地在一個細胞群體中鑒定出所有經過編輯的DNA序列。通過尋找這些熒光標簽,他們能夠實現98%的準確率。
2.Nature:利用CRISPR-Cas9鑒定出AML白血病的新藥物靶標---METTL3
doi:10.1038/nature24678
為了鑒定出治療急性骨髓性白血病(AML)的潛在新方法,來自英國韋爾科姆基金會桑格研究所、劍橋大學格登研究所等研究機構的研究人員在一項新的研究中,利用CRISPR-Cas9基因編輯技術篩選AML細胞的弱點。他們構建出攜帶著在人AML細胞中可能需要加以靶向的基因發生突變的小鼠白血病細胞,并且系統性地測試每個基因,以便發現哪些基因是AML細胞存活所必需的。
這些研究人員zui終篩選到46個潛在的候選基因,它們中的多數產生能夠修飾RNA的蛋白。在這些基因當中,METTL3是具有zui強影響的基因之一。他們發現盡管METTL3是AML細胞存活所必需的,但是它并不是健康的血細胞所必需的,這就使得它成為一種不錯的潛在藥物靶標。相關研究結構于2017年11月27日在線發表在Nature期刊上,論文標題為“Promoter-bound METTL3 maintains myeloid leukaemia by m6A-dependent translation control”。
3.Nat Commun:利用CRISPR-Cas9繪制DNA突變
doi:10.1038/s41467-017-01891-9
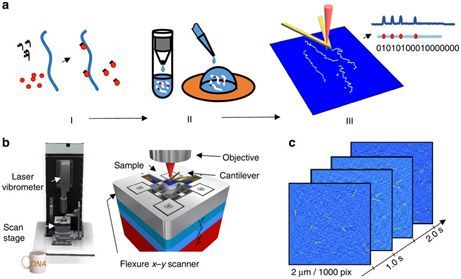
圖片來自Nature Communications, doi:10.1038/s41467-017-01891-9。
在一項新的研究中,來自美國弗吉尼亞聯邦大學的Jason Reed博士和同事們開發出一種新的納米繪圖(nanomapping)技術,這可能引發致病性基因突變診斷和發現方法變革。這種新技術將高速原子力顯微鏡(AFM)與一種基于CRISPR的化學條形碼技術結合起來,幾乎與DNA測序那樣準確地繪制DNA圖譜,同時更快地處理大片段的基因組。更重要的是,這種技術能夠由在普通的DNA播放器中發現的部件供電。相關研究結果于2017年11月21日在線發表在Nature Communications期刊上,論文標題為“DNA nanomapping using CRISPR-Cas9 as a programmable nanoparticle”。
為了證實這種技術的有效性,這些研究人員繪制出淋巴瘤患者的淋巴結活組織樣品中存在的基因易位。這些基因易位在淋巴瘤等血癌中特別普遍,但是也存在于其他的癌癥中。
4.Science:重大突破!利用細菌CRISPR/Cas系統構建出世界上zui小的磁帶錄音機
doi:10.1126/science.aao0958
在一項新的研究中,來自美國哥倫比亞大學醫學中心的研究人員通過一些巧妙的分子技術,將一種天然的細菌免疫系統轉化為一種微型數據記錄器,從而為開發將細菌細胞用于疾病診斷和環境監測等用途的新技術奠定基礎。相關研究結果于2017年11月23日在線發表在Science期刊上,論文標題為“Multiplex recording of cellular events over time on CRISPR biological tape”。
這些研究人員對人體腸道中普遍存在的大腸桿菌的一種普通的實驗室菌株進行基因修飾,使得它們不僅記錄與它們與環境之間的相互作用,而且還記錄這些事件發生的時間。
論文通信作者、哥倫比亞大學醫學中心病理學、細胞生物學與系統生物學系助理教授Harris Wang說,“這些被病人吞下的細菌可能能夠記錄它們在整個消化道中經歷的變化,從而對之前無法觀察到的現象產生的認識。”其他的應用可能包括環境監測,生態學和微生物學領域的基礎研究。
Wang和他的同事們利用很多細菌物種中存在的一種免疫系統---CRISPR-Cas---來構建這種微型數據記錄器。CRISPR-Cas系統復制來自入侵病毒的DNA片段,因此隨后的細菌后代能夠更加有效地抵抗這些病原體。結果就是細菌基因組中的CRISPR位點按時間順序記錄著在病毒感染中存活下來的細菌和它的祖先遭遇到的病毒感染。當這些相同的病毒試圖再次感染時,這種CRISPR-Cas系統能夠識別和消除它們。
5.Blood:利用CRISPR/Cas9替換T細胞受體產生優異的抗癌T細胞
doi:10.1182/blood-2017-05-787598
在一項新的研究中,來自英國卡迪夫大學的研究人員發現一種方法來提高免疫系統中的T細胞破壞癌癥的能力,從而為抵抗一系列癌癥提供新的希望。相關研究結果于2017年11月9日在線發表在Blood期刊上,論文標題為“CRISPR-mediated TCR replacement generates superior anticancer transgenic T-cells”。論文通信作者為卡迪夫大學醫學院的Andrew Sewell教授,論文*作者為Sewell實驗室的Mateusz Legut博士。
利用CRISPR/Cas9基因組編輯技術,這些研究人員對殺傷性T細胞(killer T-cells)進行進一步基因改造:移除它們的非癌癥特異性受體,并將這些受體替換為那些能夠識別和摧毀特定癌細胞的受體。
這些研究人員相信隨著時間的推移,基因編輯技術的新改進將會*改變癌癥免疫療法,*地提高它們的療效,并讓它們適用于更廣泛的不同類型的疾病患者群體。
6.Science:CRISPR戰爭突顯授予保護范圍廣泛的權問題
doi:10.1126/science.aao2468
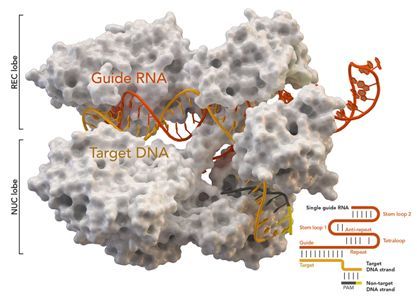
圖片來自Thomas Splettstoesser (Wikipedia, CC BY-SA 4.0)。
美國杜克大學法學教授Arti Rai和亞利桑那州立大學生物技術教授Robert Cook-Deegan在一篇知識產權政策論壇論文中談及了基因編輯戰爭。他們提出在一些產權糾紛中,相比于發明的人,法院應當有更多的考慮。以CRISPR-Cas9等技術為例,他們聲稱應當將一些想法(和權利)賦予給作為與這種技術相關的未來研究工作的受益者的公眾。相關論文發表在2017年11月17日的Science期刊上,論文標題為“Racing for academic glory and patents: Lessons from CRISPR”。
CRISPR-Cas9是一種前沿的基因編輯技術。鑒于很多研究人員正在利用它開展基因編輯研究,它一直在新聞報道中出現。但是它得到廣泛報道的另一個原因是兩方正在聲稱他們發明了它。這兩方是美國加州大學和布羅德研究所。據稱,因許可權的存在,權將為這場戰爭的zui終贏家帶來大量的收入。
正如Rai和Cook-Degan所指出的那樣,由于1980年拜杜法案(Bayh-Dole Act)的通過,諸如此類的戰爭已經進行了幾十年。拜杜法案允許實體獲得聯邦資助的研究工作成果的。在這場CRISPR戰爭中,雙方都獲得美國國家衛生研究所(NIH)的資助,并且都申請了,但是申請的時機是不明朗的。但是也正如這兩名作者所指出的那樣,在法律糾紛中不應該丟失或忽視的是公眾的權利。如果一方在這場戰爭中獲勝,那么應設法控制誰能夠使用這種基因編輯技術和以何種方式使用。在將這種*所有權授予給一個實體的情形下,法院可能以一種有害的方式阻礙基因研究。如果一組研究人員在消除一種遺傳病中正在取得進展但因不能夠獲得許可而進展緩慢,該如何處理?無辜的人可能因為法院的裁決而受到損害。這兩名作者提出解決方法就是在這些情形下,讓法院不再授予保護范圍廣泛的權,而是授予保護范圍狹窄的權,這就讓權持有者享有一些權利,但不是全部權利,從而為前沿技術創造一種更加開放的體系。
7.PNAS:“基因剪刀”改造出三眼蚊子
doi:10.1073/pnas.1711538114
據美國加州大學河濱分校近日消息,該校科學家利用“基因剪刀”工具,培育出了多個特征發生改變的埃及伊蚊,這些黃色蚊子擁有三只眼睛、翅膀發育畸形。他們希望這些由基因編輯工具改造出的蚊子,能幫助預防和控制蚊媒傳播疾病。研究發表在一期的美國《國家科學院院刊》上。
現在,研究人員對埃及伊蚊進行了基因改造,使其生殖細胞系能穩定地表達Cas9酶,這種酶在目前流行的基因編輯工具“CRISPR/Cas9”中發揮了關鍵的“剪刀”作用。之后,研究人員使用CRISPR技術,對伊蚊的DNA(脫氧核糖核酸)進行了有針對性的編輯。
研究人員對蚊子體內與表皮、翅膀和眼睛發育有關的基因進行干預或破壞,zui終培育出了黃色的、擁有三只眼睛、翅膀畸形的蚊子。比如,基因編輯工具對與表皮色素有關的基因進行干預后,蚊子從黑色變成了黃色;與眼部色素相關的基因被破壞后,蚊子眼睛的顏色也從黑色變成了白色。
8.Nat Biotechnol:重磅!科學家開發出能攜帶CRISPR系統的新型納米顆粒 可實現對細胞基因組的編輯
doi:10.1038/nbt.4005
圖片來源:MIT。
近日,刊登在雜志Nature Biotechnology上的一篇研究報告中,來自MIT的科學家開發出了一種新型納米顆粒,這種納米顆粒能夠運輸CRISPR基因編輯系統,并對小鼠機體的基因進行特異性修飾;因此研究人員就能夠利用納米顆粒來攜帶CRISPR組分,從而就消除了使用病毒的需要。
利用這種新型的運輸技術,研究者就能對大約80%的肝臟細胞進行特定基因的切割,這或許就能達到目前在成體動物中應用CRISPR技術的*成功率。 研究者Daniel Anderson教授說道,讓我們非常激動的是,我們制造了這種特殊的納米顆粒,其能被用來*特異性地編輯成年動物機體肝細胞中的DNA;本文研究中,研究者所研究的一種名為Pcsk9的基因能調節機體膽固醇的水平,而人類機體中該基因的突變或許和一種名為家族性高膽固醇血癥的罕見疾病有關,目前FDA批準的兩種抗體藥物能夠抑制Pcsk9基因的表達,然而這些抗體藥物需要在患者后半生中定期服用,而新型的納米技術或能*性地對該基因進行編輯,同時就為治療這種罕見疾病提供了新的治療思路。
9.Nat Commun:基因編輯CRISPR-Cas9研究獲新成果
doi:10.1038/s41467-017-01496-2
復旦大學生命科學學院、遺傳工程國家重點實驗室黃強課題組與盧大儒課題組合作的關于基因編輯系統CRISPR-Cas9的研究成果在線發表于學術期刊《自然·通訊》(Nature Communications)。該成果用冷凍電鏡單顆粒三維重構方法解析了CRISPR-Cas9的DNA剪切活性結構,在CRISPR-Cas9的DNA剪切機理研究方面取得了重要進展。
過去幾年,眾研究機構陸續解析了多個“Cas9-sgRNA-DNA靶鏈”的三元復合物晶體結構。然而,這些復合物結構并沒有*揭示出真正的DNA剪切活性構象,人們對CRISPR-Cas9如何通過HNH與RuvC核酸酶域切割DNA單鏈的分子機制還很不明確。因此,獲得CRISPR-Cas9的剪切活性結構成為了揭示該系統DNA剪切機理的關鍵。
針對上述研究問題,黃強與盧大儒研究團隊早在2014年就考慮采用冷凍電鏡方法來解決。他們首先構建了釀膿鏈球菌Cas9酶 (SpCas9)、sgRNA和DNA的三元復合物,然后用冷凍電鏡單顆粒三維重構方法解析該復合物的溶液結構,獲得了一個5.2埃分辨率的冷凍電鏡結構 。
復合物結構的原子模型顯示,在已解析的所有結構中,該復合物的HNH酶活性中心zui接近DNA鏈的切割位點;分子動力學模擬及點突變實驗表明,該復合物的HNH和RuvC核酸酶活性中心的催化氨基酸可以與DNA解旋單鏈形成切割反應所需構象。因此,研究獲得的復合物結構是CRISPR-Cas9的DNA剪切激活構象,為全面揭示剪切機理提供了關鍵的活性結構信息,并為應用蛋白質工程技術優化該系統、降低其脫靶效應提供了重要的結構生物化學基礎。目前,研究團隊正在所得結構的指導下,應用蛋白質設計方法對CRISPR-Cas9系統進行優化,以開發脫靶效應低、編輯效率高的新型基因編輯系統。
10.Nat Genet:新方法可校正CRISPR篩選的癌癥基因依賴性數據中的假陽性
doi:10.1038/ng.3984
在一項新的研究中,布羅德癌癥依賴性圖譜(Broad Cancer Dependency Map)團隊將來自342種癌細胞系的基于CRISPR的數據添加到他們不斷增加的癌癥基因依賴性目錄中,并且提供一種新的方法來確保這些數據的準確性。相關研究結果于2017年10月30日在線發表在Nature Genetics期刊上,論文標題為“Computational correction of copy number effect improves specificity of CRISPR–Cas9 essentiality screens in cancer cells”。
為了限制這些假陽性結果,布羅德癌癥依賴性圖譜計劃---一個將來自布羅德癌癥項目的阿喀琉斯計劃團隊和癌癥數據科學團隊、布羅德研究所基因擾動平臺和其他的布羅德研究所團隊的研究人員召集在一起的聯合計劃---開發出一種被稱作CERES的計算方法,該方法可對匯集的CRISPR篩選數據進行拷貝數效應校正,并且針對癌細胞的基因依賴性提供給一種無偏見的看法。
正如布羅德癌癥依賴性圖譜團隊在這項研究中報道的那樣,他們利用CERES對來自342種癌細胞系的全基因組CRISPR-Cas9篩選數據(迄今為止產生的zui大CRISPR敲除數據集)進行校準,這些癌細胞系是由布羅德-諾華癌細胞系百科全書(Broad-Novartis Cancer Cell Line Encyclopedia, CCLE)進行管理的。這種方法極大地降低這些數據中的假陽性結果,準確地找到了已知的基因依賴性(如KRAS基因突變),并且允許新的基因依賴性浮現出來。
11.PNAS:中科院科學家培育出基因編輯瘦肉豬
doi:10.1073/pnas.1707853114
中國科學家23日宣布,他們利用基因編輯方法培育出一批健康的瘦肉豬,比正常豬脂肪少24%。這項工作由中國科學院動物研究所趙建國領導完成,論文發表在新一期美國《國家科學院學報》上。一些專家認為,這是一個重要進展。但也有人懷疑民眾對基因編輯瘦肉豬的接受程度。
趙建國研究團隊通過新一代基因編輯工具CRISPR,向豬細胞內插入一種叫解偶聯蛋白1(UCP1)的基因,減少脂肪沉積,增加瘦肉率,zui終培育出的豬比正常豬脂肪少24%。
他們通過基因編輯工具將UCP1基因定點整合到豬胎兒的成纖維細胞的基因組中,培育出2500多個克隆豬胚胎,然后將這些胚胎注入13只代孕母豬體內,其中3只母豬懷孕并產下12只雄性仔豬。與野生型豬相比,這些仔豬體溫調節能力顯著增強,但脂肪率和膘厚度顯著降低,瘦肉率顯著提高。分析表明,UCP1基因主要通過促進脂肪水解來減少脂肪沉積,降低脂肪率。
12.Genome Biol:上海生科院完整敲除研究獲進展,可選擇性消除單條染色體
doi:10.1186/s13059-017-1354-4
11月25日,《基因組生物學》發表了題為《CRISPR/Cas9介導的基因編輯技術敲除目標染色體》的研究論文,該研究由中科院神經科學研究所、腦科學與智能技術創新中心、神經科學國家重點實驗室楊輝研究組與北京大學胡家志實驗室合作完成。該研究介紹了CRISPR/Cas9技術的新型應用,即在細胞、胚胎或體內組織中,針對目標染色體進行多個DNA剪切,可以選擇性消除單條染色體。CRISPR/Cas9介導的目標染色體消除為動物模型的建立以及非整倍體疾病的治療提供了新的策略與方法。
II型細菌的CRISPR/Cas9系統由Cas9 核酸酶和單鏈引導RNA(sgRNA)組成,已經被改造成一個的基因編輯工具,能顯著地提高編輯基因組的能力。sgRNA引導Cas9到達特定的基因組區域,剪切形成雙鏈DNA缺口,該缺口可以通過兩種方法修復——非同源染色體末端連接修復或同源重組修復。CRISPR/Cas9基因編輯技術已經應用于生產基因突變、重組和染色體片段敲除的細胞或動物。而研究者提出CRISPR/Cas9基因編輯技術是否可以用于整條染色體的消除,進而對建立染色體缺失的動物模型以及非整倍體疾病的治療提供新的途徑。
為了驗證這個想法,研究人員首先證明應用CRISPR/Cas9介導的針對Y染色體的多位點DNA切割可以有效地將小鼠胚胎干細胞的Y染色消除。這種多位點剪切可通過單個sgRNA靶向結合多個特異的染色體位點,或者通過14個sgRNA分別結合各自的特異位點來達到。此外,他們還發現小鼠X染色體,人的7號和14號染色體都可以通過這種方法消除。更為重要的是,唐氏綜合癥病人的iPS細胞中的21號染色體也可以通過這種方法特異性消除。因此,該研究*次證實了性染色體和常染色體可以通過基因編輯特異性消除。
13.Genome Res:世界*!科學家培育出帶有基因剪刀的工具豬
doi:10.1101/gr.222521.117
11月16日,中國科學院廣州生物醫藥與健康研究院賴良學課題組的研究成果“Cre-dependent Cas9-expressing pigs enable efficient in vivo genome editing”在線發表在Genome Research(《基因組研究》)上。該研究構建了新型條件性表達Cas9基因工具豬模型,利用此模型,實現了直接對成體大動物進行體內基因編輯,并建立了大動物原發性肺癌模型。
研究人員利用基因打靶技術,成功地將能夠剪開基因的Cas9蛋白基因插入到豬基因組的一個特定的位點(ROSA26),相當于在豬體內加入了一把基因剪刀,并且在Cas9基因附近加上了能與Cre重組酶結合的loxp位點,后者相當于一個開關,能對其剪切功能的開啟加以控制。研究人員利用此工具模型,不需要依賴受精卵注射或體細胞核移植技術,在動物體內轉入能識別特定基因的gRNA和重組酶,就可直接對豬的基因組進行編輯,從而快速獲得相應基因編輯豬模型。
研究人員將包裝的含有Cre重組酶和靶向六種腫瘤相關基因的gRNAs慢病毒通過滴鼻方式,感染工具豬的肺臟,在豬肺細胞的基因組發生癌化突變。三個月后,豬出現了典型的肺癌癥狀和病理變化,從而成功地建立了原發性肺腫瘤大動物模型。
14.FEBS J:艾滋病新突破,CRISPR基因編輯技術再立一大功艾滋病新突破,CRISPR基因編輯技術再立一大功
doi:10.1111/febs.14293
在對抗艾滋病的道路上,*的科學家們一直在努力著,這些年來,對抗艾滋病的療法也取得了很大的進展。艾滋病之所以可怕是因為艾滋病毒會通過摧毀人類的免疫系統而傷害感染者的身體,感染艾滋病毒的患者基本上都不是因為艾滋病毒而死,而是由于殘缺的免疫系統使他們變得“遍體鱗傷”。據研究,艾滋病毒會感染大腦中的某些細胞,這些細胞是小膠質細胞,同時,被感染的小膠質細胞釋放有毒和炎性分子,削弱或殺死周圍的神經元,引起神經認知障礙的問題。
長久以來,研究人員一直在尋找方法,了解艾滋病毒引起的神經認知障礙,然而,始終沒有大的進展,研究人員對于艾滋病病毒和小膠質細胞作用的了解非常有限。然而,發表的一項研究提供了新的見解,在新的研究中,科學人員使用CRISPR / Cas9基因編輯技術,開發了一種新型的艾滋病毒感染小膠質細胞模型。
研究人員在報告中表示:“在此次研究中,我們運用CRISPR / Cas9基因編輯技術所設計的新模型,有助于我們了解由艾滋病毒引起的神經認知障礙,這一發現將會帶來治療艾滋病的新策略。”(生物谷 Bioon.com)
 您好, 歡迎來到化工儀器網
您好, 歡迎來到化工儀器網

 12
12


