分子膠的篩選案例詳解_MedChemExpress(MCE 中國)

分子膠的作用機制是什么?已知的分子膠是如何被發現以及改造優化的?為什么 CRBN 類分子膠的研究熱度最高?AI 能否助力分子膠的發現?本期小 M 將就這些問題帶大家一探究竟~
分子膠(Molecular Glues)是一類能夠誘導蛋白質-蛋白質相互作用的小分子,近年來可謂是醫藥圈的‘香餑餑’。據不全統計,2020 年以來禮來、輝瑞等各大藥企在分子膠領域已經完成 24 筆大的交易,整體交易規模加起來高達 270 億美元。它們不僅擴展了‘不可成藥’靶點的治療潛力,還為癌癥、神經退行性疾病等難治性疾病提供了新的解決方案。
Section.01
分子膠的作用機制是什么?
如圖 1,分子膠通常通過誘導蛋白質相互靠近發揮作用,即誘導或增強兩種蛋白質之間的相互作用。這可能會產生多種生物學效應,包括:(A) 降解靶蛋白(通過誘導靶蛋白與 E3 連接酶相互靠近);(B) 穩定靶蛋白-效應蛋白復合物的結構;(C) 抑制酶的活性 (通過阻斷靶蛋白酶與其下游活動所需的 Native binding partner 的結合);(D) 激活靶蛋白的活性 (通過促進靶蛋白與調節蛋白的相互作用,增強靶蛋白的活性)。
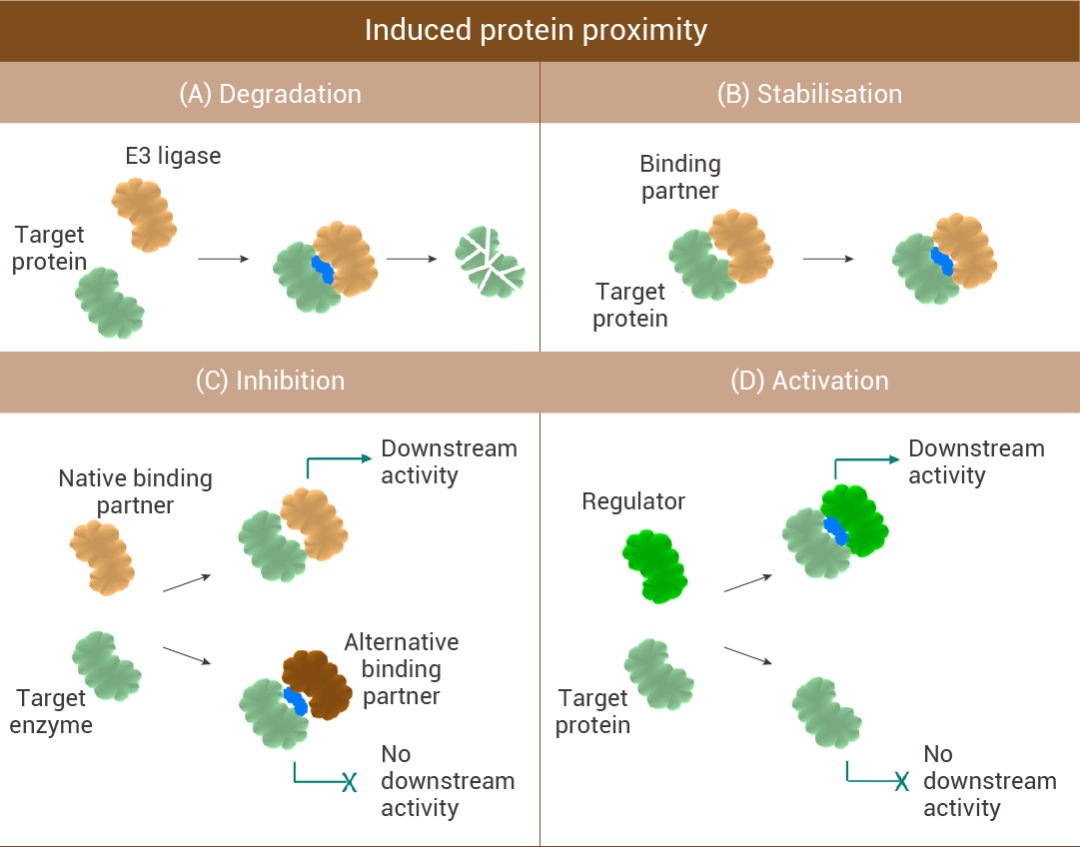
圖 1. 分子膠誘導蛋白相互作用功能示意圖[1]。
Section.02
已知的分子膠是如何被發現
以及改造優化的?
小 M 為大家整理了 3 類高效篩選分子膠的案例,其基本研究思路為:① 構建分子膠類似物化合物庫; ② 通過高通量篩選獲得苗頭分子; ③ Western blot 驗證被降解的目標蛋白; ④ AlphaScreening 或 NanoBit 實驗檢測蛋白-蛋白相互作用; ⑤ HiBiT 實驗檢測蛋白含量以獲得 DC50 (半數降解濃度) 和 Dmax (最大降解率)。
利用高通量表型篩選出一類分子膠降解劑,該分子膠可以誘導胎兒血紅蛋白 (HbF) 的表達,為治療鐮狀細胞病等血紅蛋白相關疾病提供了新的候選藥物。
研究人員開發了一種基于高通量流式細胞術的表型篩選方法,使用人源 CD34+ 細胞衍生的成紅細胞作為實驗模型來篩選胎兒 HbF 誘導劑。研究人員篩選了一個包含 2,814 種基于 CRBN 的分子膠類似化合物庫,發現了一組能夠增加 HbF 陽性細胞比例的化合物 (如圖 2),同時不影響成紅細胞的增殖和分化。這種表型在之前已知的 HbF 誘導劑類別中很少見。
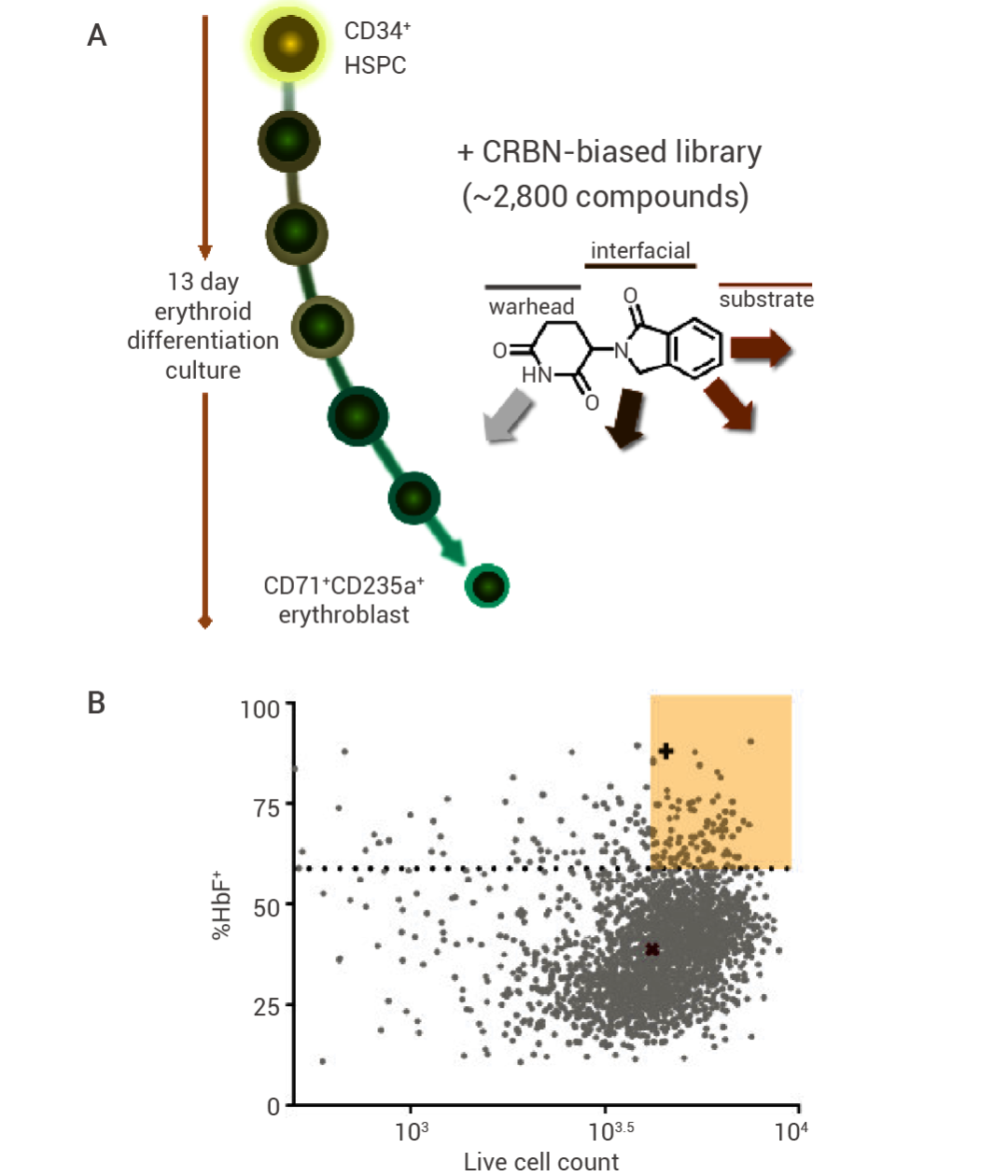
圖 2. 表型篩選流程與結果分析[2]。
隨后進一步基于全局蛋白質組學分析識別出在化合物 1 的處理下顯著變化的蛋白質,圖 3A 表明化合物 1 是通過 CRBN 依賴性降解轉錄因子 WIZ,進而驅動了體外 HbF 誘導。圖 3B 表明化合物 1 能夠顯著降解 WIZ 并誘導 HbF,因此被選為優化的起點。
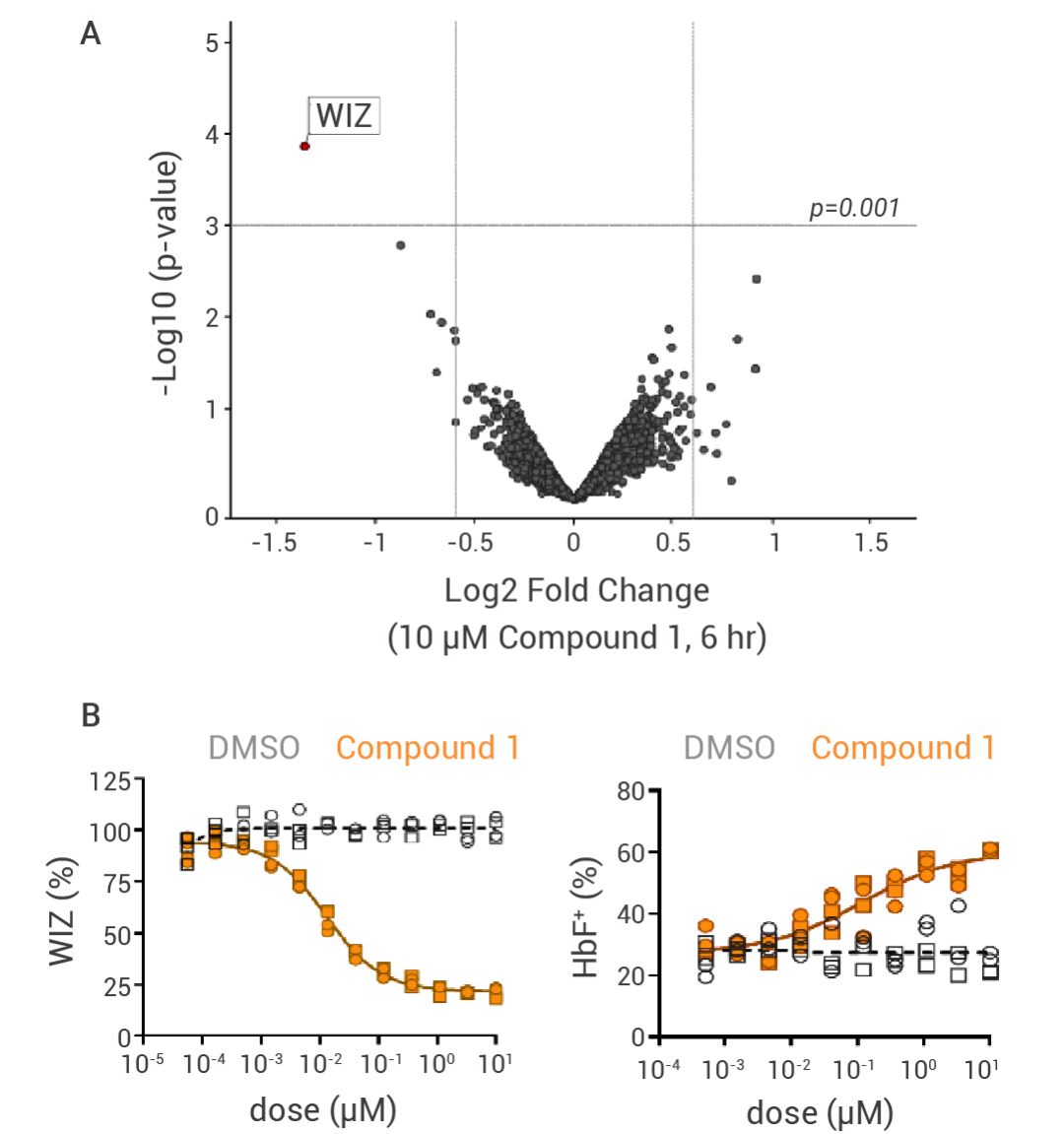
圖 3. 驗證化合物 1 的作用靶點[2]。
(a) log2 (倍數變化) 和 p 值的雙重標準,確保篩選結果的可靠性和顯著性),(b) 體外活性分析。
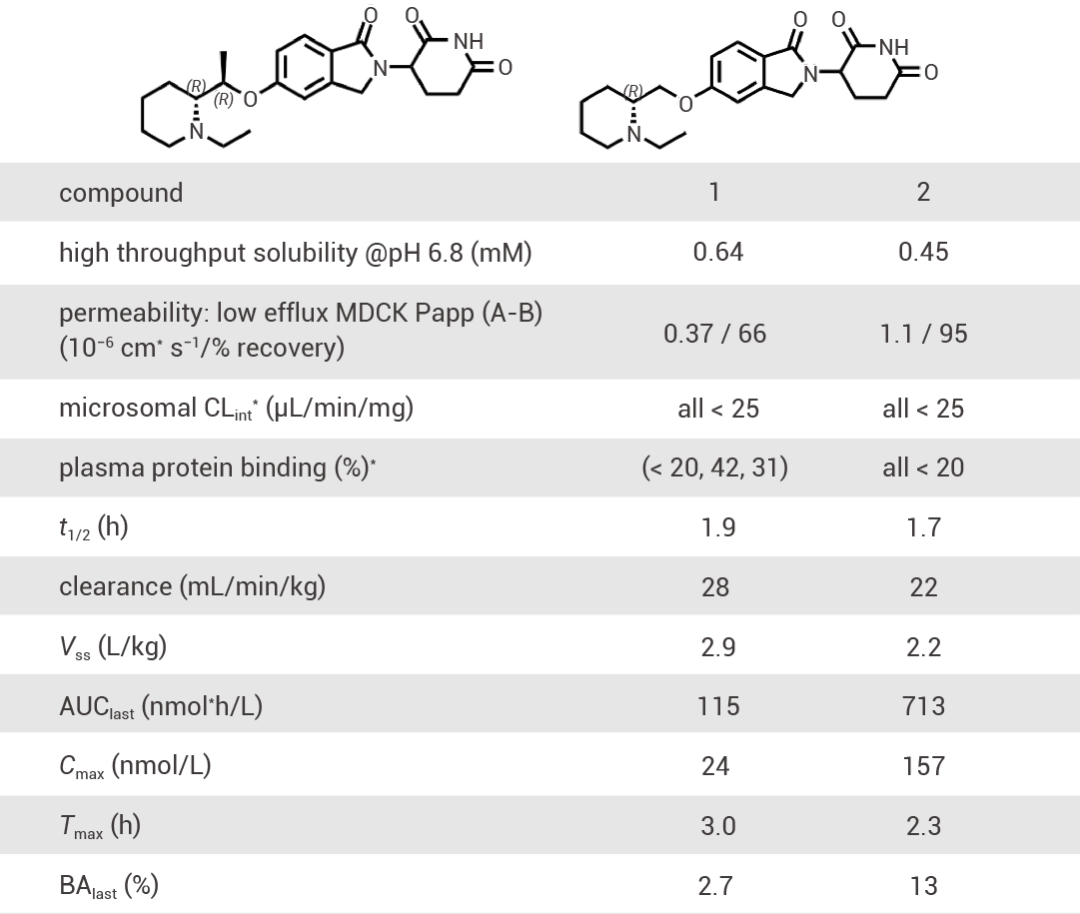
接下來,研究人員對化合物 1 進行了簡單的改造得到化合物 2,該化合物同樣能夠以 CRBN 依賴的方式強效誘導胎兒 HbF 并降解 WIZ,隨后研究人員進一步評估化合物 1 和化合物 2 的理化性質和藥代動力學性質,如圖 4 所示,化合物 2 表現出更好的口服生物利用度 (BA%last = 12%),因此后續以化合物 2 作為進一步開發的先導分子。
表 1. 化合物 1 和化合物 2 的 ADME/PK 數據[2]。
戊二酰亞胺是 CRNB 分子膠降解劑的關鍵片段,研究人員開發一種利用多組分反應作為核心模塊化步驟合成含戊二酰亞胺分子膠庫的方法。通過對合成的化合物庫進行篩選發現了靶向酪蛋白激酶 1α (CK1α) 和 Wee 樣蛋白激酶 (WEE1) 的分子膠降解劑。并且通過分子對接和結構分析,為進一步優化分子膠提供結構基礎。
研究人員首先設計了一種新的化學合成策略,即利用 GBB 反應 (Groebke?Blackburn?Bienayme,一種多組分縮合反應) 作為最后一步關鍵的合成步驟,快速高效地獲得 200 多個結構多樣的 CRBN 分子膠庫。
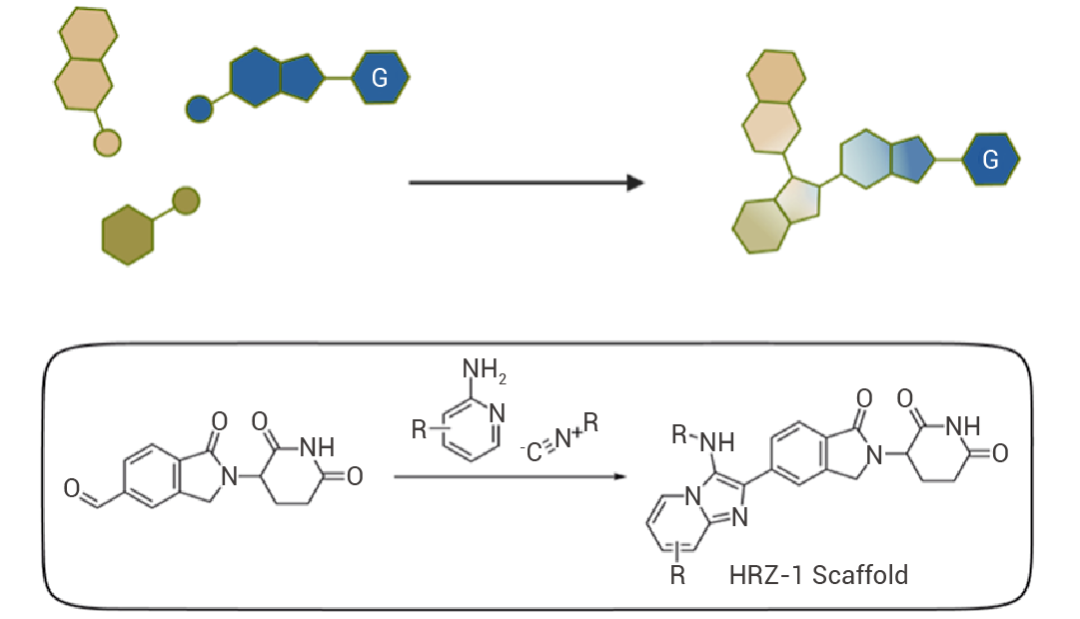
圖 4. 基于多組分反應 (GBB reaction) 一步合成含 HRZ 骨架的化合物庫[3]。
隨后,研究人員在 CRBN 野生型和 CRBN 敲除的 MOLT-4 細胞 (人白血病細胞) 中進行 72 小時的細胞存活率實驗,以篩選出以 CRBN 依賴性方式誘導強效抗增殖的化合物,結果找到 3 個苗頭分子,其中化合物 2 的 EC50 低于 5 nM,化合物 1 和 3 的 EC50 分別為 12 nM 和 139 nM。
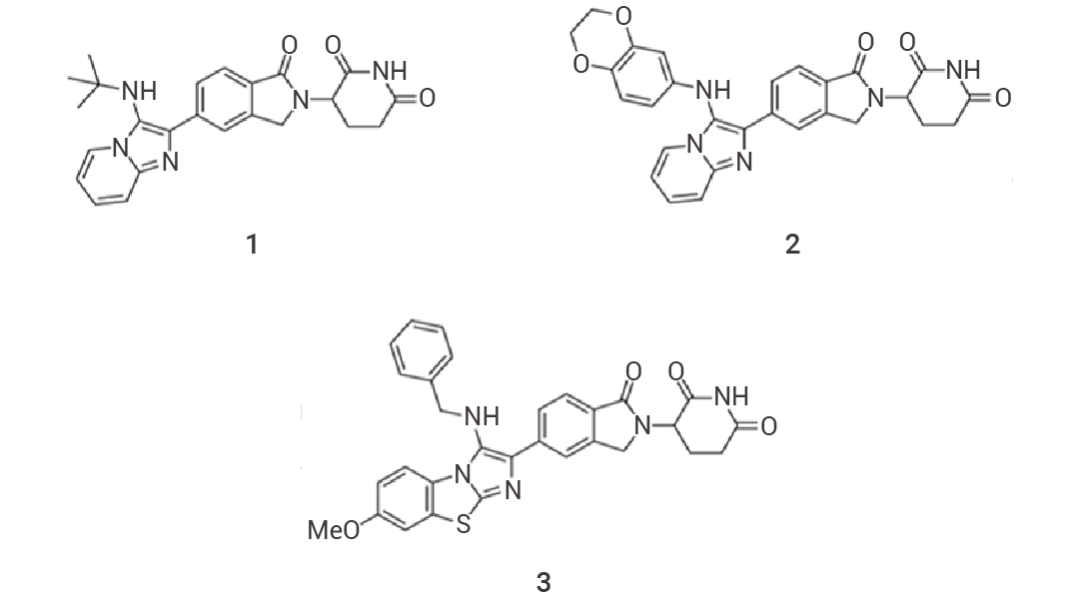
圖 5. 3 個苗頭分子結構[3]。
接下來,研究人員基于化合物 2 來識別靶點,通過全細胞蛋白質組學分析 (whole-cell proteome profiling) 檢測化合物 2 處理 MOLT-4 細胞 5 小時后的蛋白變化,發現 CK1α (酪蛋白激酶 1α) 和 WEE1 (細胞周期調控激酶) 是主要降解靶點,并通過 Western blot 確認化合物 1,2,3 是 CRBN 依賴的 CK1α 和 WEE1 降解劑。
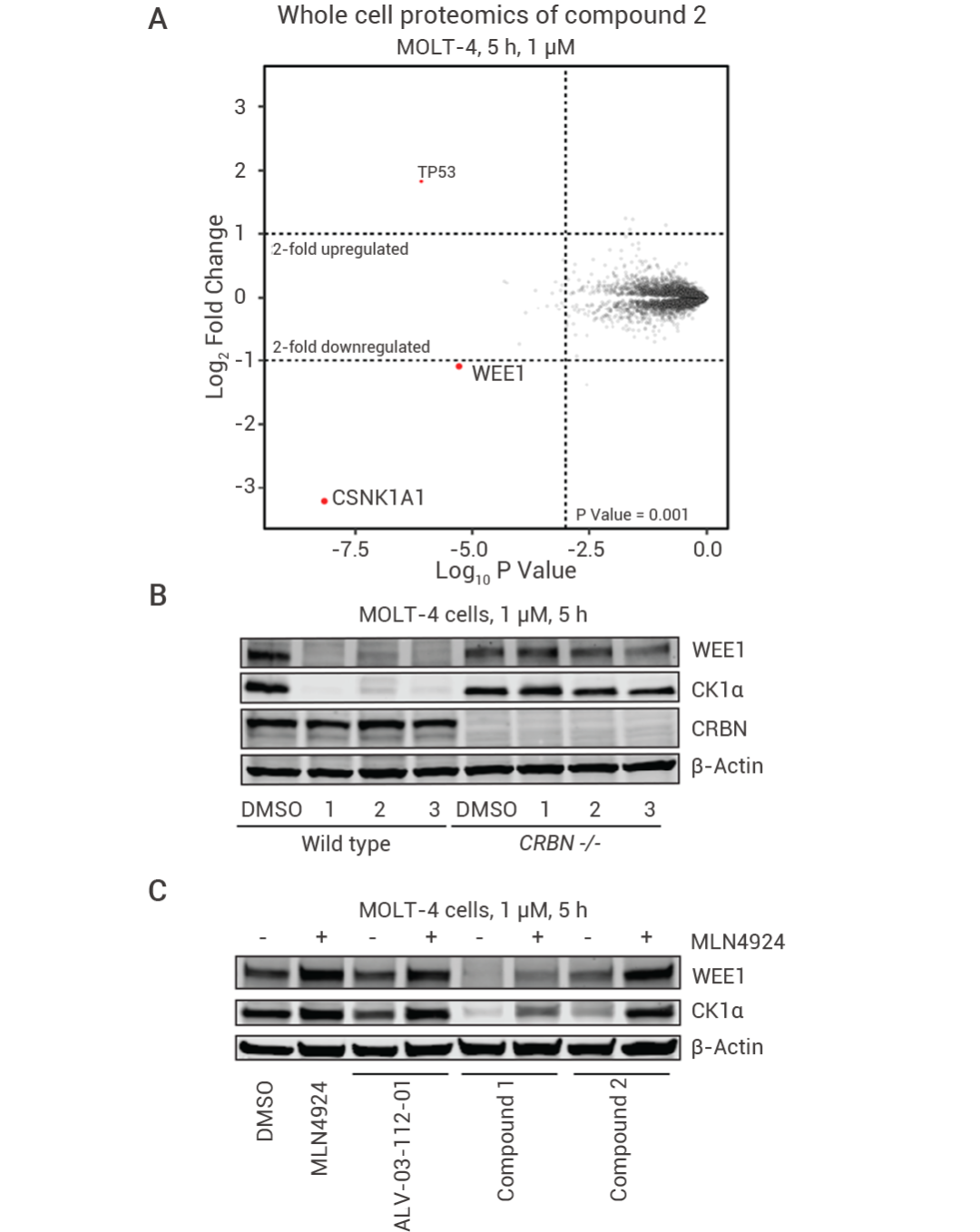
圖 6. 全細胞蛋白組學結果分析圖 (CSNK1A1 即為 CK1α) 以及 Western blot 驗證圖[3]。
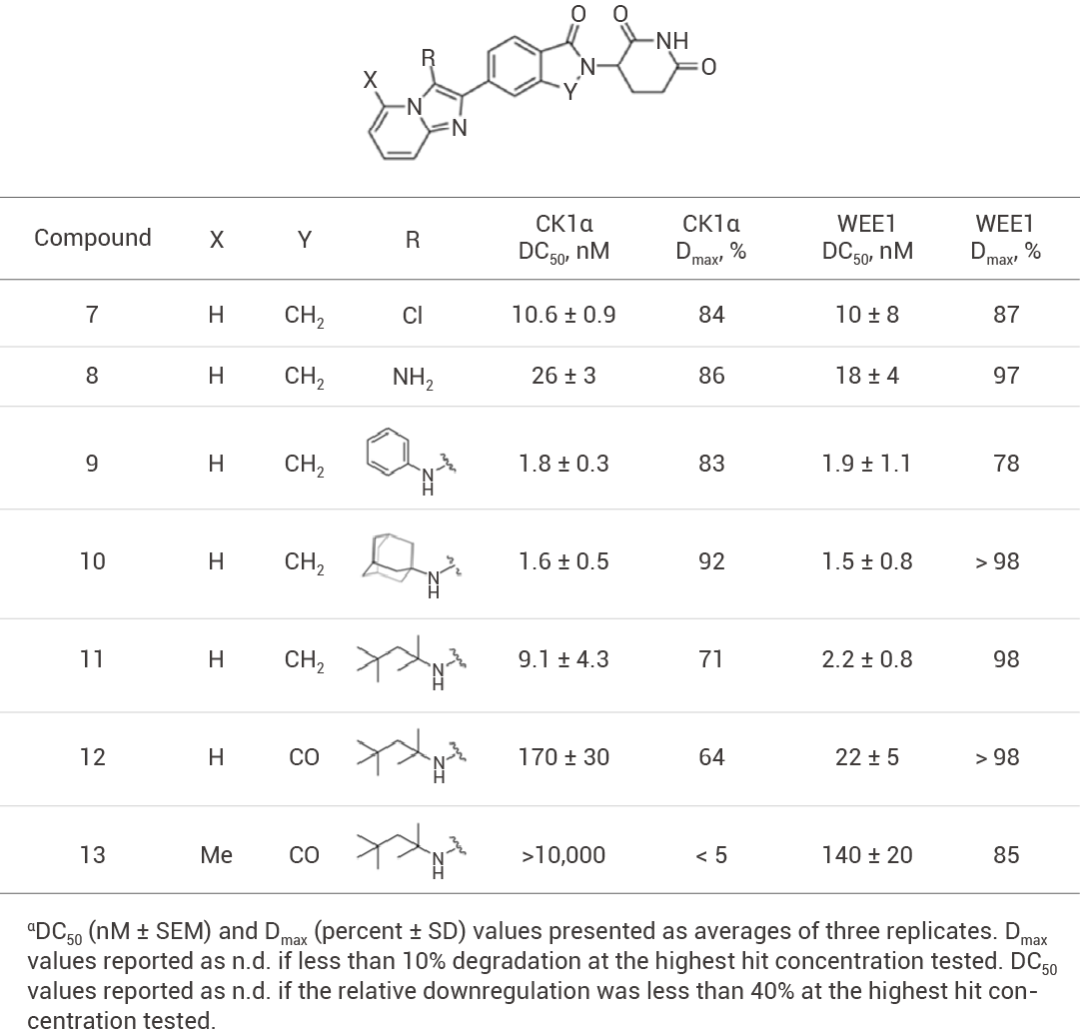
隨后研究人員開始進行結構優化,以化合物 1 作為改構起點。為了方便構效關系分析,研究人員引入 HiBit 標簽,以定量監測 Jurkat 細胞 (T 細胞白血病細胞) 中內源性 WEE1 和 CK1α 蛋白的水平,將經過改造的細胞系與不同濃度的化合物一起孵育 5 小時,然后通過終點熒光素酶測定法來檢測靶點的降解情況獲得 DC50 和 Dmax。改構主要基于傳統的藥化改構思路,圍繞化合物 1 的骨架進行較小的改動,以獲得活性和選擇性更好的化合物,最終得到化合物 10 是活性好的分子。
表 2. HRZ-1 骨架苯胺取代基的 SAR 分析[3]。
值得一提的是,研究人員還通過實驗驗證了 2 個重要的問題,第一個問題是已報道的認為 CRBN 分子膠都是通過一個由含有甘氨酸殘基的 β 發夾環 (G loop) 的降解標簽基序來與新底物結合的,研究人員分別測試了化合物 10 對野生型 WEE1 (WEE1-WT)、甘氨酸 322 突變為丙氨酸的 WEE1 (WEE1-G322A) 以及甘氨酸 322 突變為天冬酰胺的 WEE1 (WEE1-G322N) 的降解變化,結果和已報道的結論一致,WEE1-G322N 突變阻止了 WEE1 的降解。
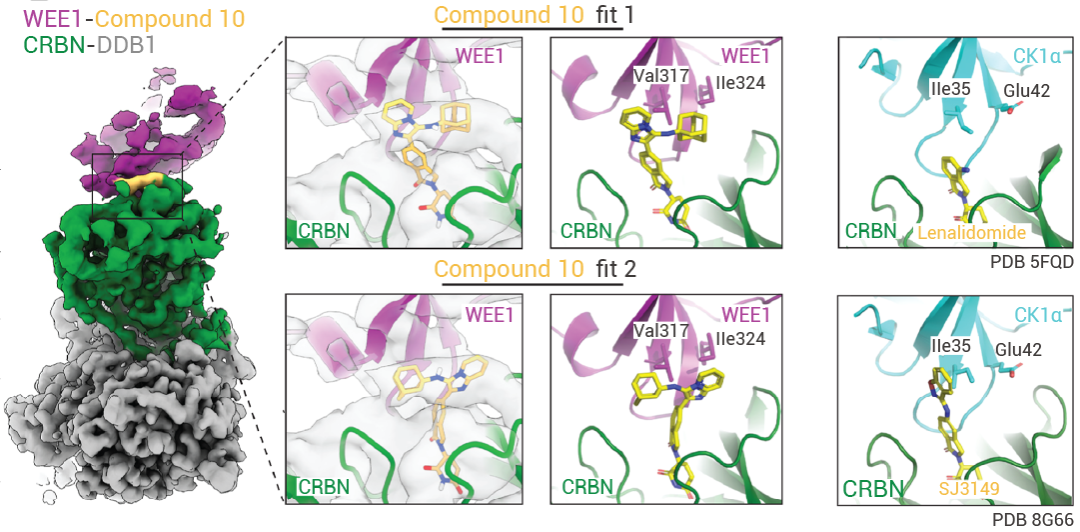
第二個問題是化合物 10 是如何介導 WEE1 與 CRBN-DDB1 結合,通過 cryo-EM 獲得 WEE1-化合物 10-CRBN-DDB1 的復合物結合模式,結果顯示 WEE1 的 G loop 對介導三元復合物的形成很重要。與此同時,盡管化合物 10 具有高親和力,但它與復合物的結合并沒有使整個復合物變得剛性。如圖 7,化合物 10 主要存在兩種可能的構象,且通過對化合物 13 進行分子對接顯示:化合物 10 和 13 的 pose 基本和 fit1 一致。作者又將 WEE1-化合物 10-CRBN-DDB1 復合物與已報道的 DDB1-CRBN-SJ3149-CK1α 復合物結構進行疊合。在化合物 10 的兩種可能結合模式中,咪唑并吡啶和金剛烷基取代基都與 SJ3149 的苯并惡唑部分部分重合,這為進一步優化分子膠提供結構基礎。
構建靶向 VHL 的 CIP-DEL 篩選文庫,該文庫包含約 938,730 個化合物。開發一種基于親和力的 CIP-DEL 篩選方法,利用“呈遞蛋白比率”來理性篩選具有高協同性的小分子化合物,對分子膠的發現具有重要意義。
諾華的研究人員參考已報道的 BRD7/BRD9 降解劑 VZ185 的 VHL 配體的連接方式,通過酚氧基團構建基于三嗪的多樣化 DEL 文庫,DNA headpiece 和 DNA tag 連接在靶向 VHL 配體的遠端酰胺上。
基于三輪建庫,第一輪在三嗪和靶向 VHL 的配體之間引入 13 種連接子,第二輪和第三輪分別在三嗪骨架上引入 290 種和 249 種不同分子砌塊,最終構建了一個包含 938,730 個分子的 DEL 篩選文庫。
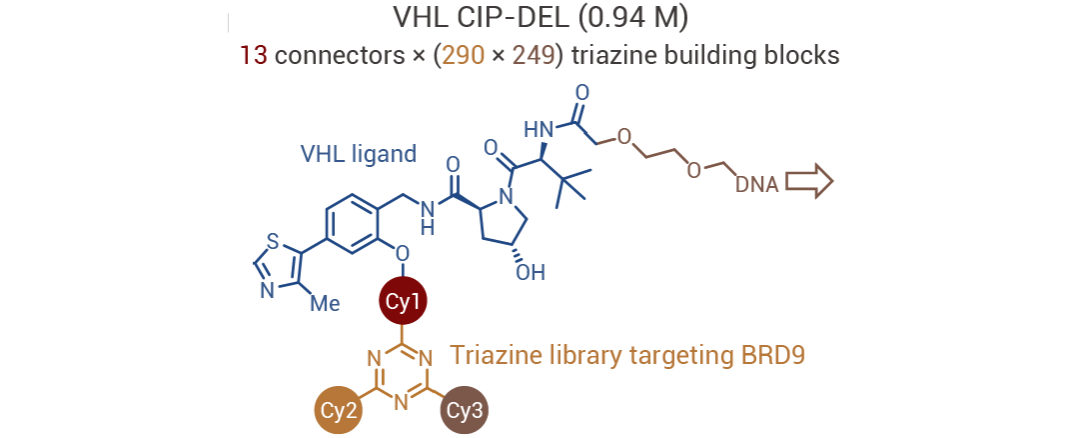
圖 8. VHL CIP-DEL 文庫核心骨架[4]。
在 CIP-DEL 篩選試驗中,首先將 His-tag 的 BRD9 (靶蛋白) 固載在磁珠上,并使用 2 種不同的實驗方法來鑒定潛在的分子膠。如圖 10 所示,將文庫和固載的 BRD9 蛋白孵育 (允許形成二元復合物),文庫首先和 VCB (VHL–elongin C–elongin B) 預孵育,再和固載的 BRD9 蛋白孵育 (允許形成三元復合物)。為了控制非特異性結合,在不存在 BRD9 的情況下,將文庫和磁珠孵育。洗滌 3 次后,加熱使蛋白質變性以釋放結合物,再將 DNA 條形碼進行 PCR 擴增和測序以鑒定結合物的結構。
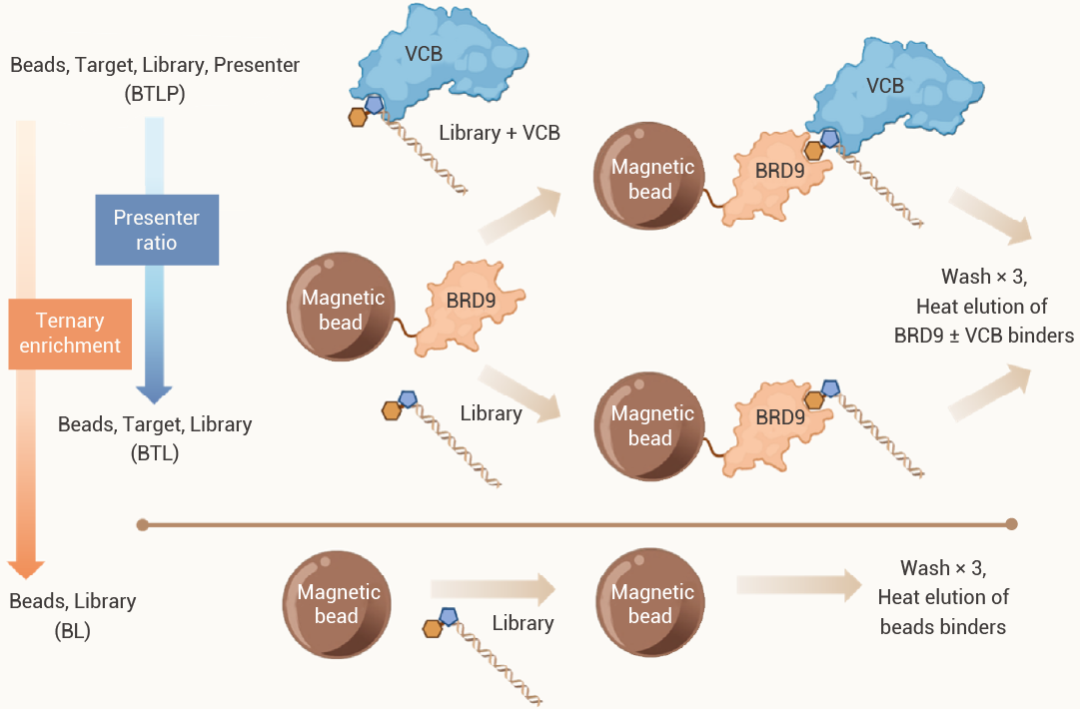
圖 9. DEL 篩選流程[4]。
為了計算富集,研究人員將 DNA 條形碼的計數數據建模為 Poisson 抽樣,通過這種建模方式,研究人員能根據總樣本計數對各個計數進行歸一化處理,同時也會考慮到測序數據的不確定性。二元富集度通過 BTL 的計數值除以 BL 的計數值來計算,三元富集度通過 BTLP 的計數值除以 BL 的計數值來計算,而呈遞蛋白比率則通過 BTLP 的計數值除以 BTL 的計數值來計算,本質上得到的是三元富集度與二元富集度的比值。呈遞蛋白比率越高,表明 CIP-DEL 化合物與 BRD9 的結合越依賴于 VCB 的存在,這意味著該化合物具有更高的協同性。研究假設可以利用呈遞蛋白比率來篩選在與 BRD9 和 VCB 形成三元復合物時具有不同協同程度的小分子。
如圖 11,研究人員將結果分為三類:第一類是三元復合物富集度高但呈遞蛋白比率低 (主要是帶有 9 號連接子 (珊瑚色) 和 12 號連接子 (藍色) 化合物),第二類是三元復合物富集度中等和呈遞蛋白比率中等的化合物 (11 號連接子 (黃色) 化合物),第三類是三元復合物富集度低和呈遞蛋白比率高的化合物 (主要是 13 號連接子 (綠色) 化合物)。
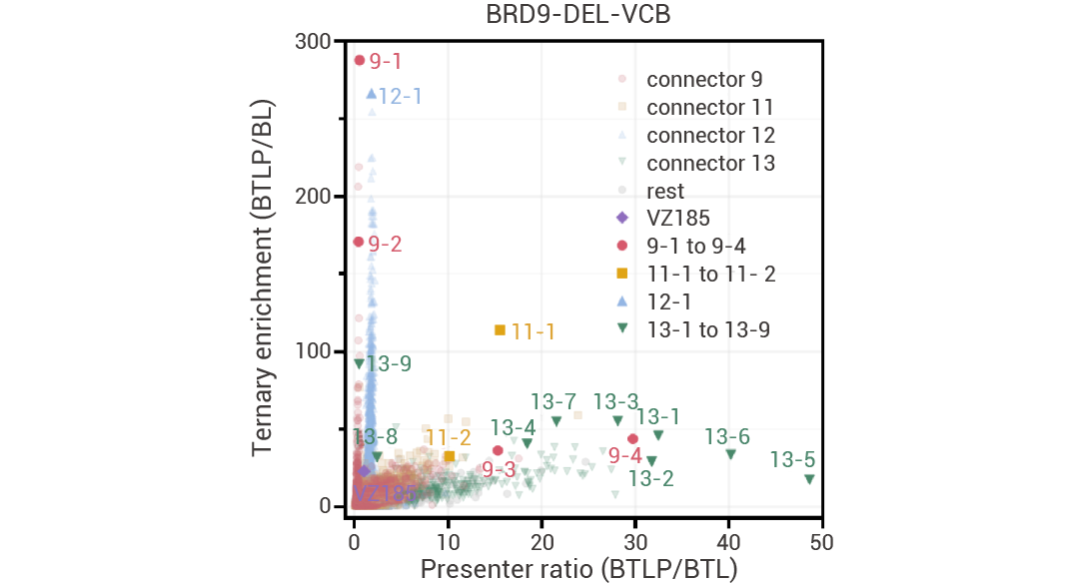
圖 10. 三元復合物富集度與呈遞蛋白比率的關系圖[4]。
后續通過 AlphaScreen 進行協同性驗證,發現化合物 13-3 和 13-7 無鉤狀效應。在細胞實驗驗證中,13-7 在 NanoBiT 實驗中誘導三元復合物形成且無鉤狀效應,在 HiBit 實驗中對 BRD9 的降解也無鉤狀效應,且具有較好的選擇性。
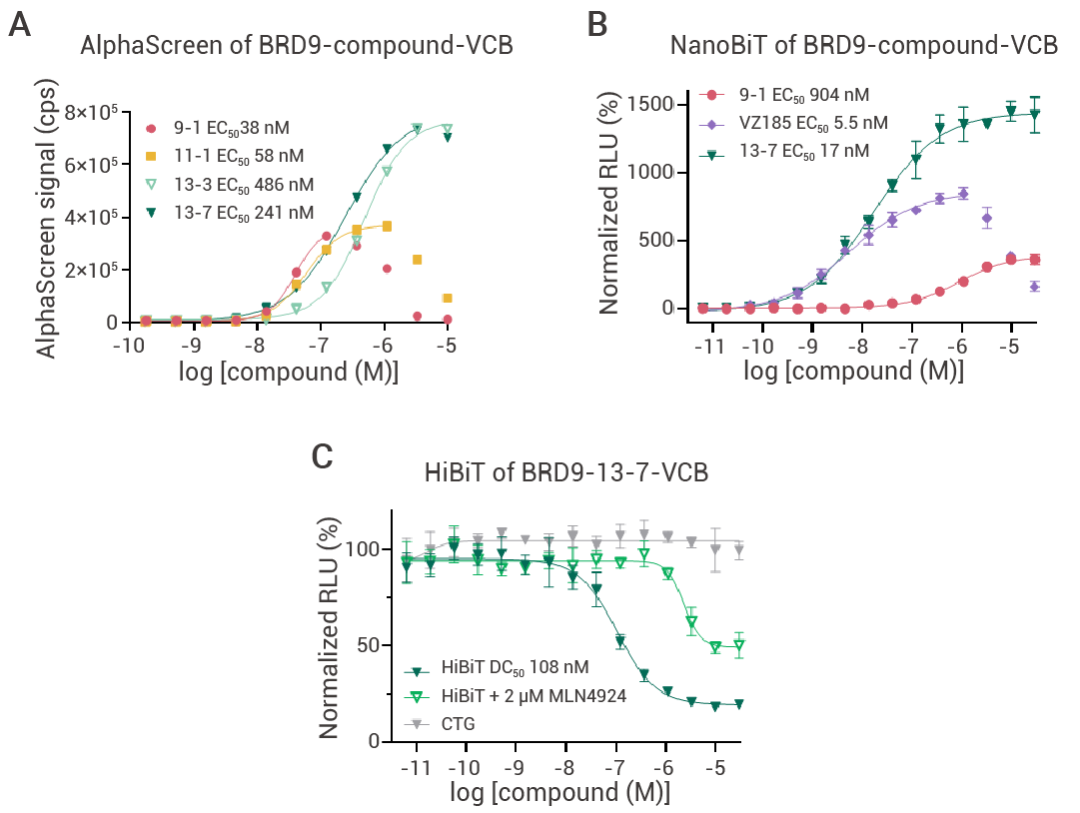
圖 11. AlphScreen, NanoBiT 和 HiBiT 實驗結果圖[4]。
Section.03
為什么 CRBN 類分子膠的
研究熱度最高?
一家專注于分子膠降解劑開發的公司 Monte Rosa Therapeutics 對 CRBN 的底物進行了更廣泛的探索。已知的 Neo-substrate 有 CK1α、GSPT1、IKZF1、IKZF2、WIZ 等,這些都是傳統意義上的難成藥靶蛋白。這些 Neo-substrate 通過一個 G-loop 與 CRBN/CELMoD 結合,G-loop 由 β-hairpin α-turn 構成,在特定位置有一個共同的甘氨酸,因此也被稱為 β-hairpin G-loop。
研究人員首先以 CK1α 的 β-hairpin G-loop 作為查詢模板 (該模板由 I35 到 E42 八個氨基酸組成,包含 5 個上游殘基 (G-5) 和 2 個下游殘基 (G+2)),在蛋白質結構數據庫 (PDB) 和 AlphaFold2 (AF2) 預測的人類蛋白質中進行搜索。選擇與查詢模板的均方根偏差 (RMSD) 小于 0.75? 且與 CRBN 無空間位阻基序,并去除其中主要定位于細胞外的蛋白質,最終確定了 1,424 種含有 CRBN 兼容 β-hairpin G-loop 的蛋白質。除此之外,還發現一種新的 helical G-loop 基序,存在于 184 種蛋白質中,進一步擴展了 CRBN-neosubstrate 的范圍。
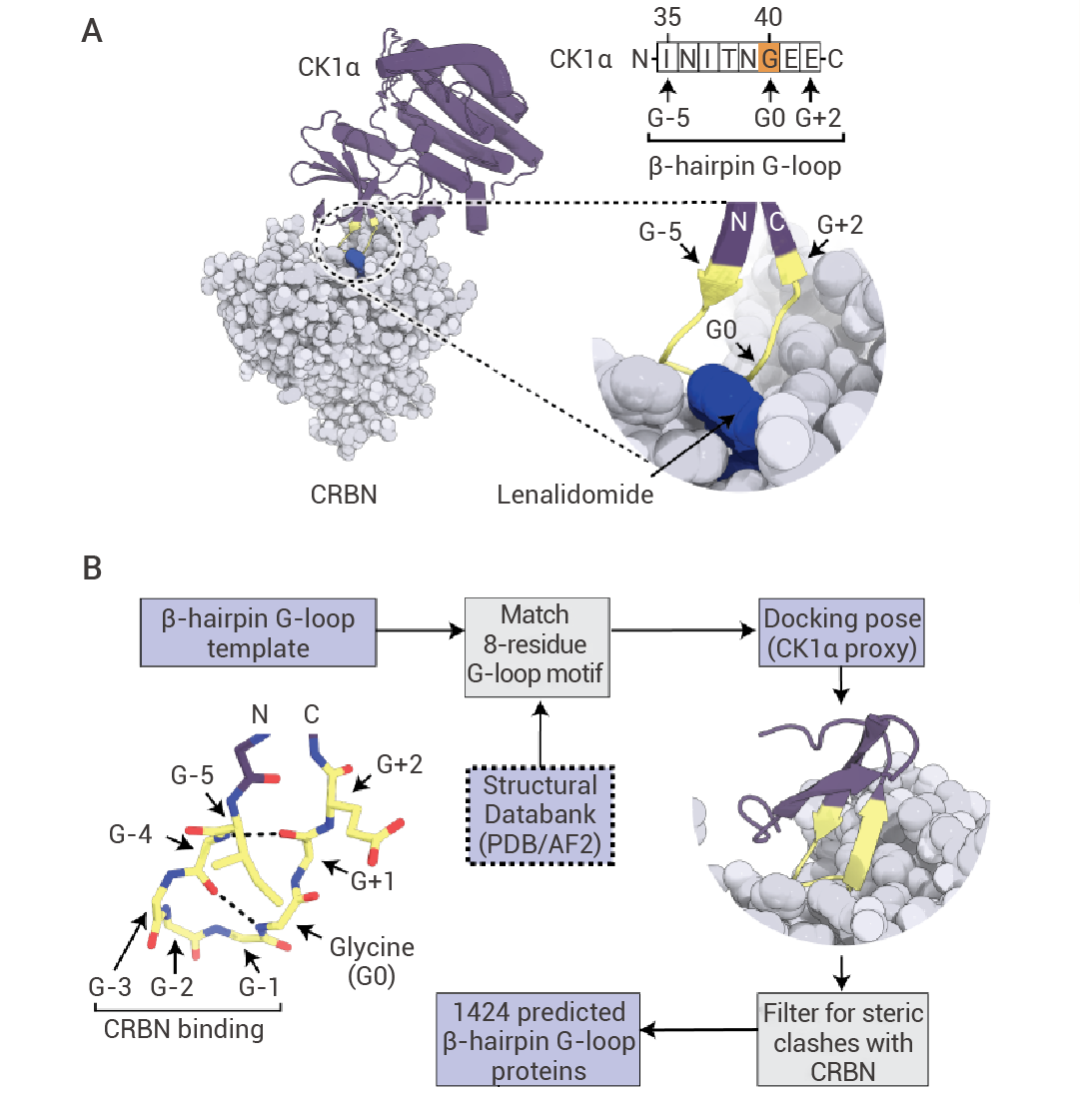
圖 12. β-hairpin G-loop 模版數據挖掘示意圖[5]。
Section.04
AI 能否助力分子膠的發現?
一直以來,分子膠的計算評估是一大難點,這包括三元復合物結構難以準確預測,DC50 和親和力難以有很強的相關性。
3 月 22 日,VantAI 給制藥行業帶來了振奮人心的消息,推出 NEO-1 模型,該模型被譽為藥物研發領域一款具有開創性的人工智能模型。NEO-1 不僅能夠預測生物分子結構,還能從頭生成分子,尤其是具備從頭生成分子膠方面的能力。大家感興趣可以去進一步了解 vant.ai/neo-1。截止今日,該模型還無法試用且無公開的文獻,小 M 很期待該模型能公開,到時跟大家再進一步分享。

圖 13. 歷代結構預測模型能力[6]。
MCE 一站式藥篩平臺聚焦于藥物發現早期,可為客戶提供多樣化的分子膠化合物庫 (HY-L918 & HY-L137),HY-L918 分子膠類似物庫由基于CRBN,VHL和DCAF14的分子膠類似物構成。同時可提供 DEL 定制和篩選服務,蛋白定制服務,表型篩選服務以及分子膠的合成定制服務等,為科研客戶及新藥研發客戶提供—站式分子膠發現及研究服務。
產品推薦 |
類藥多樣庫 Plus 由 80,000 種類藥化合物組成。本多樣性庫具備新穎性、類藥性,結構多樣性等特點,庫中化合物可重復供應,是新藥研發的有力工具,可以廣泛地應用于高通量篩選 (HTS) 和高內涵篩選 (HCS)。 |
5K Scaffold Library 由 5,000 種類藥化合物組成,每種化合物代表一種結構骨架,保證了庫的結構多樣性。庫中的化合物均經過 MedChem & PAINS filters 篩選,剔除了不合適的化學結構,避免“目標錯誤”。本庫化合物數量少但結構足夠多樣,是藥物篩選的有力工具。 |
Natural Product-like Compound Library 由 5,000 個類天然產物化合物組成,庫中每個分子含有天然產物關鍵骨架 (42 個) 或者和天然產物的谷本相似系數 >0.6,且 Natural-likeness scoring >-2。該化合物庫同時具備類藥性和新穎性,庫中化合物可重復供應,是新藥研發的有力工具,可以廣泛地應用于高通量篩選 (HTS) 和高內涵篩選 (HCS)。 |
RNA Binding Library 由 5,000 多個具有潛在 RNA 相互作用活性的小分子化合物組成,我們收集了 PDB、R-BIND、ROBIN 和內部數據庫中的已知 RNA 靶向小分子作為陽性數據集,并基于 ROBIN 數據集獲得非靶向 RNA 的小分子作為陰性數據集。基于 GeminiMol 預訓練模型,對這些分子進行編碼,并通過 Mordred 計算了 1,700+ 分子描述符作為模型的輸入。接著用 13 個深度學習模型對這些數據進行學習,所有模型都取得了良好的訓練結果,AUROC 均超過 0.75。選擇分類好的 Finetune 模型(AUROC 值:0.82,預測準確率:0.76)對 HY-L901P 進行篩選。進一步基于 StaR Rules(cLogP≥1.5,Molar Refractivity≥4,Relative Polar Surface Area≤0.3)進行再過濾,該庫同時具備結構多樣性,是 RNA 靶向藥物開發的有利工具。 |

[1] Holdgate, Geoffrey A. et al. SLAS Discovery, Volume 29, Issue 2, 100136
[2] John Ryan Kerrigan, Noel M.et al. Journal of Medicinal Chemistry 2024 67 (22), 20682-20694
[3] Hlib Razumkov.et al. Journal of the American Chemical Society 2024 146 (46), 31433-31443
[4] Liu S.et al. J Am Chem Soc. 2023 Oct 25;145(42):23281-23291
[5] Georg Petzold.et al. bioRxiv 2024.10.07.616933

免責聲明
- 凡本網注明“來源:化工儀器網”的所有作品,均為浙江興旺寶明通網絡有限公司-化工儀器網合法擁有版權或有權使用的作品,未經本網授權不得轉載、摘編或利用其它方式使用上述作品。已經本網授權使用作品的,應在授權范圍內使用,并注明“來源:化工儀器網”。違反上述聲明者,本網將追究其相關法律責任。
- 本網轉載并注明自其他來源(非化工儀器網)的作品,目的在于傳遞更多信息,并不代表本網贊同其觀點和對其真實性負責,不承擔此類作品侵權行為的直接責任及連帶責任。其他媒體、網站或個人從本網轉載時,必須保留本網注明的作品第一來源,并自負版權等法律責任。
- 如涉及作品內容、版權等問題,請在作品發表之日起一周內與本網聯系,否則視為放棄相關權利。
 手機版
手機版 化工儀器網手機版
化工儀器網手機版
 化工儀器網小程序
化工儀器網小程序
 官方微信
官方微信 公眾號:chem17
公眾號:chem17
 掃碼關注視頻號
掃碼關注視頻號
















 采購中心
采購中心