固有柔腦膜側支化對缺血性卒中后快速血流募集的影響
柔腦膜側支狀態可獨立預測卒中結果。美國和日本研究人員Atsushi Kanoke等使用光學相干斷層掃描血管造影術,通過比較固有軟腦膜側支化程度不同的兩種品系小鼠,確定了缺血性卒中后側支流動和下游血液動力學的時空動態。發現C57BL/6小鼠大腦中動脈(MCA)閉塞后,立即檢測到柔腦膜側支血流的強勁補充,并在7天內持續。而Balb/C小鼠在MCA閉塞期間和之后一天,都幾乎沒有觀察到側支血流募集,雖然閉塞后7天皮質灌注略有提高,但還是造成了更大的梗塞面積和更差的卒中結果。兩品系小鼠在MCA閉塞后30min內,穿透性小動脈(PA)的血流量都減少了90%以上,其中Balb/C小鼠的血流量減少更顯著,恢復更少。此外,與Balb/C小鼠MCAO閉塞后,毛細血管通過時間的不均勻性也較C57BL/6小鼠延長更多。表明皮質卒中后,固有柔腦膜側支的范圍會影響下游的血液動力學,并對微血管床產生長期影響。研究成果以“The impact of native leptomeningeal collateralization on rapid blood flowrecruitment following ischemic stroke"為題發表于Journalof Cerebral Blood Flow & Metabolism。
背景
威利斯環(CW)和柔腦膜(LMA)血管網分別包含初級和次級側支通路。其中LMA側支可能涉及向大腦皮層表面提供雙向動脈血液、連接大腦前動脈(ACA)和大腦中動脈(MCA)、大腦中動脈(MCA)和大腦后動脈(PCA),并在較小程度上連接ACA和PCA。當CW下游的大腦動脈突然閉塞時,需要招募以上血管招募來維持血液供應。大量證據表明缺血性卒中后的LMA側支化可作為卒中結果的有力預測指標。因此在急性缺血性卒中患者治療管理中,通過神經成像技術評定側支流動狀態已成為一項可靠的決策評估,且已經ESCAPE臨床驗證。已知年齡、血管風險和遺傳因素都能影響側支的發育及動態應答,但對于影響腦血管側支化的因素并不*明了。
通過比較近交品系小鼠,對影響固有LMA側支程度的遺傳因素已經有了很好的研究,并已用于預測MCA卒中后的梗死體積。同源圖譜確定該遺傳變異為Dce1。Dce1等位基因滲入Balb/ C基因組可使野生型Balb/C小鼠軟腦膜側支恢復83%,并在大腦中動脈閉塞(MCAO)后以等位基因依賴的方式恢復腦血流、減少梗塞體積,證實了固有側支對缺血區腦血流灌注的重要性。
盡管一直固有側支循環與急性缺血性卒中后腦損傷的嚴重程度間存在既定聯系,但尚不清楚LMA側支系統補償腦血流的時間模式,以及它如何影響缺血性卒中后下游較小血管的血液供應。由于沒有適當的方法,許多臨床前研究無法評估滋養動脈對缺血區域的貢獻,只能依賴于評估整體血液灌注或yiti檢查。本研究假設LMA側支程度減小、先前存在的LMA側支直徑減小會影響卒中后血液從軟腦膜血管灌注到微血管床,使用光學相干斷層掃描血管造影術(OCTA)評估皮質的腦血流動力學(圖1)。使用固有LMA側支發育程度不同的兩種小鼠品系C57BL/6和Balb/C,確定了缺血性卒中后LMA吻合周圍的空間和時間動力學。還描述比較了不同側支血流對下游穿透小動脈和毛細血管中血流的影響,以及不同側支血流對卒中結果的影響。
圖1 OCT系統和OMAG方法示意圖。(a)1310 nm SD-OCT系統設置示意圖。(b)OMAG掃描方案。一個cluster執行八次重復掃描,OMAG算法提取血流信息。400幀形成一個OMAG體積。(c)3D OMAG體積的正面MIP。(d)使用DOMAG算法獲得的速度B幀。(e)雙向軸向速度圖。彩色條表示從大腦下行(負,綠色)和上行(正,紅色)血流的紅細胞軸向速度,在±6.1mm/s范圍內。(f)大腦皮層中下行的PA血流(頂部)和上行的小靜脈血流(底部)。(g)X-Y平面矩形切片(頂部)和帶有穿過平面的PA和小靜脈血流信號的矩形切片(底部)。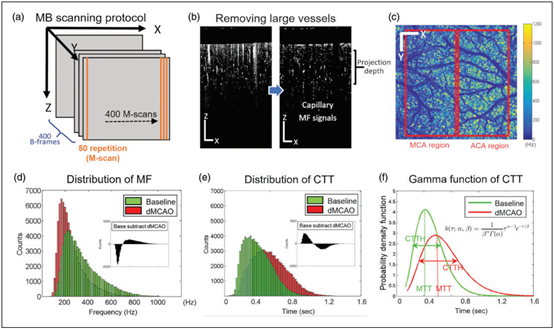
圖2 OCT毛細血管測速法示意圖。(a)OCTA測速掃描協議示意圖。(b)掩模對毛細血管血流信號的作用。大于15μm的血管腔被去除掉了。(c)毛細血管中頻(MF)圖,由300μm深度的3D頻率信號的正面投影生成。(d)MF分布及基線與dMCAO間的差異。(e)毛細血管通過時間(CTT)的分布及基線與dMCAO間的差異。(f)在基線和dMCAO時的Gamma函數。
結果
01-固有柔腦膜的側支化是卒中后快速逆向血流募集的原因
為確定固有側支如何在空間和時間上影響逆行血流,用寬視野Doppler OCT成像并量化遠端MCA和ACA血流。基線時,檢測到MCA分支的流速從近端(S3)到遠端(S1)梯度減小(圖3a-c),而兩品系的血管直徑保持相對恒定(圖3d)。dMCAO后30 min,C57BL/6小鼠中觀察到強勁的MCA血流逆轉以及連接遠端MCA和ACA的彎曲側支吻合,而Balb/C小鼠中沒有(圖3b)。dMCAO過程中,最靠近ACA和MCA間連接點的遠端MCA小動脈(圖3a中S1和S2)的血流速度顯著降低,C57BL/6組降到其基線值的56%和31%,Balb/C組降低更顯著,達基線值的0.2%和1.7%。此后C57BL/6組在dMCAO后7天,MCA小動脈更近端段(S3)的流速和流量逐漸恢復了2-3倍(圖3b、c和e)。而Balb/C組S1和S2段的流速、血管直徑和流量在dMCAO后7天才顯示出程度明顯的恢復,可見功能性血流(圖3c-e)。使用DOCT評估的不同品系間MCA遠端小動脈中LMA血流募集的應變差異,與激光多普勒血流計(LDF)評估的MCA區域的局部腦血流量(rCBF)差異相關(圖3f),表明側支血流的范圍可預測缺血區域的整體血流灌注狀態。
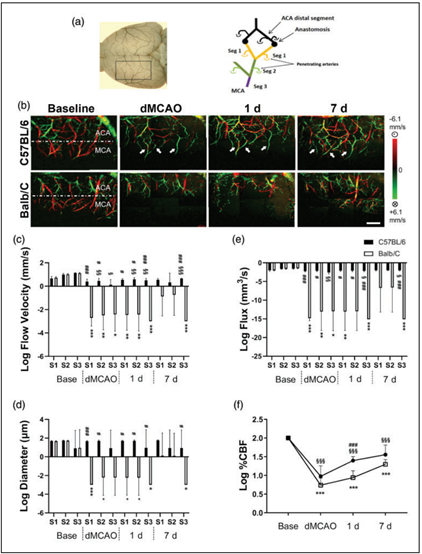
圖3 C57BL/6小鼠MCA遠端閉塞后,從ACA快速募集逆行側支血流,但Balb/C小鼠沒有。(a)DOCT成像區域,對應大腦背面染色灌注的軟腦膜血管圖像。圖示三個MCA遠端分支的命名及其與MCA和ACA的相對位置。(b)C57BL/6和Balb/C小鼠基線(Base)、MCAO期間30min(dMCAO)、MCAO后24h和7天(7d)的代表性DOCT圖像。流向掃描探針束或ACA區域的血流為紅色,流向近端MCA的逆行血流為綠色。白色箭頭表接受來自ACA逆行血流的MCA分支。(c)C57BL/6和Balb/C小鼠的三個遠端MCA段的流速、血管直徑(d)和流量(e)的對數柱狀圖。基線時,兩品系的流速、血管直徑或流量無顯著差異。但C57BL/6小鼠MCA的遠端分支通過吻合被ACA逆行血流灌注,從紅色到綠色反向流動。最靠近MCA主干的Seg3段的軸向流速和流量在MCAO后隨著時間推移逐漸增加。相反Balb/C組由于LMA側支網絡發育不良,在MCAO期間和之后24h幾乎沒有顯示逆行血流,導致MCA區域的流量一直顯著少于C57BL/6組。(f)LDF測定的閉塞部位的rCBF顯示血液灌注隨時間逐漸改善。在MCAO后第一天,不同品系間rCBF恢復情況差異顯著。
02-Balb/C小鼠中,卒中引起的MCA區域PA血流量減少會進一步加劇
使用高分辨率Doppler OCT確定逆行的軟腦膜側支血流如何影響下游穿透小動脈(PA)的血流。在直徑5mm的顱窗內進行掃描,覆蓋ACA和MCA區域,獲得OMAG和DOMAG掃描及正面流速圖譜(圖4a)。發現在MCAO后30min,C57BL/6和Balb/C小鼠MCA區域的總PA流量都顯著減少,分別減至基線水平的約13.7%和0.03%(圖4a和b)。盡管C57BL/6小鼠在同一時間點的LMA血流減少較緩和,但得到的數據與之前結論一致,即PA是大腦循環的瓶頸。C57BL/6小鼠MCA區域的PA血流在dMCAO后7天逐漸恢復到基線的49.3%,而Balb/C小鼠在同一時間點僅恢復到6.7%(圖4b)。品系間總流量的差異也反映在dMCAO階段未閉合PA的平均橫截面直徑上(圖4c)。兩品系小鼠dMCAO期間都檢測到ACA區域總流量減少,隨后7天內分別恢復到基線的72%和64%(圖4e)。C57BL/6小鼠MCA區域PA的最大流速在dMCAO期間和dMCAO后7天顯著高于Balb/C小鼠(圖4d),而dMCAO期間兩品系ACA區域的趨勢相反(圖4g)。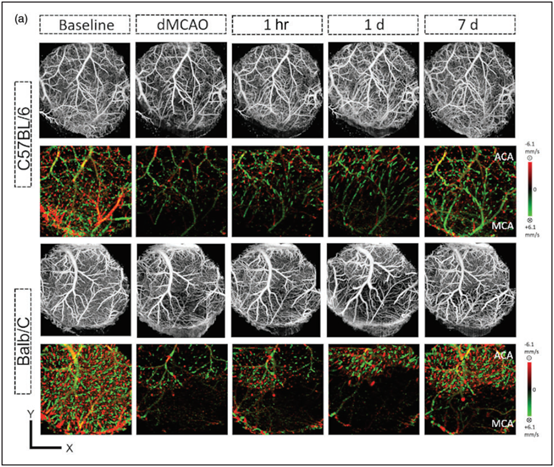
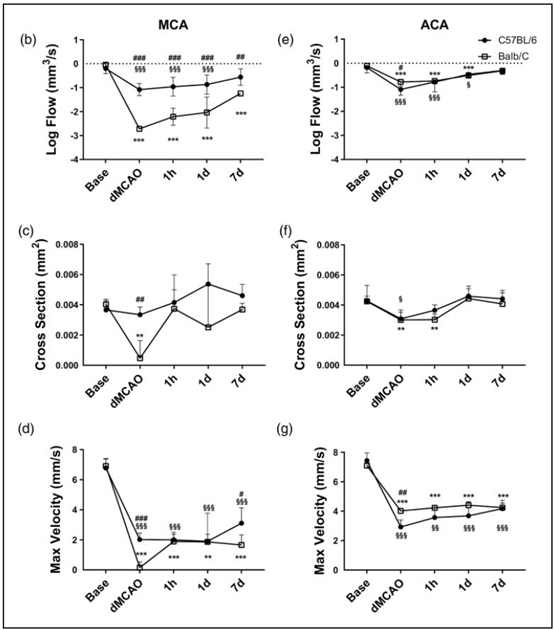
圖4 卒中后Balb/C小鼠MCA區域PA血流幾乎耗盡,恢復很少。(a)兩品系小鼠皮質表面下300 μm厚的組織內,OMAG數據的正面MIP(上圖)和3D雙向DOMAG數據的正面MIP(下圖)。軸向速度范圍:±6.1 mm/s。確定了每個品系中MCA(b-d)和ACA(e-g)區域內總流量、平均橫截面積和最大軸向流速的動態變化。
03-Balb/C小鼠卒中后毛細血管通過時間的不均勻性較C57BL/6小鼠更顯著
評估并比較了兩品系dMCAO后毛細管通過時間的平均值和空間分布。在遮蔽直徑大于15μm的血管后,通過OCTA測速儀獲得毛細管平均頻(MF)圖譜(圖5a)。從圖2c紅色方框的MCA和ACA區域MF信號中推導出通過時間的空間分布特征,包括平均毛細血管通過時間(CTT)和毛細血管通過時間不均勻性(CTTH)。Balb/C小鼠在dMCAO后30min平均CTT增加,并在MCA區域頸總動脈閉塞(CCAO)血流逆轉后1h持續,而ACA區域在dMCAO期間及后1天,平均CTT增加(圖5b和d),品系間無顯著差異。Balb/C小鼠中,卒中引起的CTTH增加一直持續,且dMCAO期間MCA區域的增加顯著多于C57BL/6組(圖5c和e),導致卒中后微血管阻力增加、氧提取減少。Balb/C小鼠ACA區域的CTTH在dMCAO后也增加了,但在隨后的7天恢復。品系間ACA區域的CTTH無顯著差異(圖5e)。
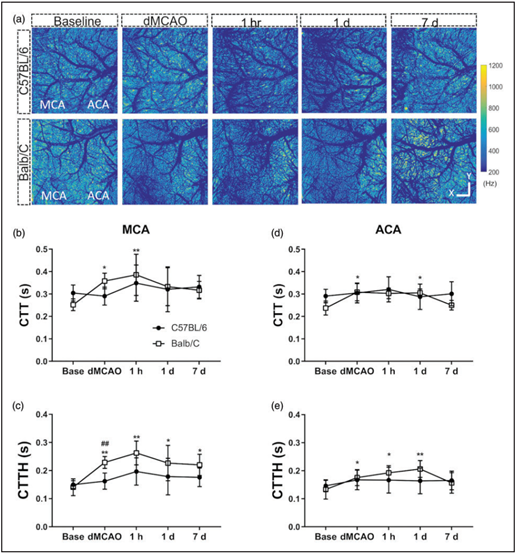
圖5 Balb/C小鼠卒中后,毛細血管通過時間的空間不均勻性顯著大于C57BL/6小鼠。(a)通過皮質內3D頻率信號正面投影生成的毛細血管平均頻率圖。Balb/C小鼠MCA(b)和ACA(d)區域的平均毛細血管通過時間(CTT)在dMCAO后顯著增加,并持續至CCAO逆轉后。卒中后CTTH增加,MCA區域(c)一直升高,Balb/C小鼠ACA(d)區域直到dMCAO后1天前一直升高。Balb/C小鼠dMCAO期間,CTTH的增加顯著多于C57BL/6小鼠。
04-C57BL/6和Balb/C小鼠固有腦血管的遺傳變異
為確定缺血性卒中后固有LMA側支的范圍是否有助于逆行血流補償,分析了DiI標記的動脈造影。基線時,C57BL/6小鼠ACA和MCA間相互連接的LMA吻合明顯多于Balb/C小鼠(圖6a和b),與以前的報告一致。而Balb/C小鼠PcomA開放性顯著好于C57BL/6小鼠(圖6c)。在三個不同神經軸水平上,兩品系從中線到ACA和MCA區域邊界的距離相似(圖6d),表明兩品系小鼠大腦背半球MCA的相對面積相似,與以前的發現一致。
05-柔腦膜血流的快速募集可使梗死體積和神經損傷更小
C57BL/6小鼠在dMCAO后7天,梗死面積較Balb/C小鼠減少更多、水平階梯和轉角測試評估的運動功能更好,表明快速LMA血流募集預示著更好的卒中結果(圖6e-g)。雖然Balb/C小鼠的血流流量和rCBF在dMCAO后7天有所改善,但這種晚期血流募集并不能挽救已經因缺血而損失的腦組織,也不能改善卒中后的功能性結果。
圖6 MCAO前固有柔腦膜側支的范圍可預測C57BL/6和Balb/C小鼠的卒中結果。(a)兩品系小鼠動脈造影背視圖。放大插圖顯示C57BL/6小鼠MCA和ACA血管網之間有許多吻合點,但Balb/C小鼠沒有。(b)MCA和ACA在基線時連接側支的量化。(c)兩品系小鼠Pcom開放性的評分和比較。(d)三個不同神經軸水平上測定中線與ACA和MCA吻合線之間的距離。(e)Balb/C小鼠卒中后7天的卒中面積仍顯著大于C57BL/6小鼠。與卒中后7天的C57BL/6小鼠相比,Balb/C小鼠在高架水平梯測試(f)時滑過更頻繁,轉角測試(g)中同側轉彎明顯更多,反映出在感覺運動不對稱方面有更明顯的功能損傷。
結論
本研比較了兩種具有不同側支程度的近交系小鼠,證明了固有LMA側支對快速側支血流動力學影響非常大,預先存在的固有側支化程度與卒中后快速LMA血流補償和下游血流動力學改善有關。shouci使用DOMAG表明實驗室動物中,卒中引發的LMA側支招募取決于固有側支循環的范圍,還進一步闡明了LMA側支血管下游的血液動力學變化,確定了MCAO反應中軟腦膜血管對快速和延遲血流募集的不同機制。
雖然以上研究證明側支循環范圍或狀態與缺血性損傷之間存在很強的相關性,但也存在獨立于側支循環、可調節梗塞體積的基因,表明缺血性損傷的生物反應仍十分復雜。研究還表明單獨的血管新生對治療或預治療缺血性卒中可能效果不大;開放度較低的小血管的增加不會改善灌注情況,需要適當大小的側支動脈血管,與治療性血管重建領域觀點一致,即與血管新生相比,動脈新生(小動脈大小的增加)是一種更好的替代方法。
參考文獻:The impact of native leptomeningeal collateralization on rapid blood flow recruitment following ischemic stroke. Journal of Cerebral Blood Flow & Metabolism (2020):0271678X2094126.
 您好, 歡迎來到化工儀器網
您好, 歡迎來到化工儀器網
